Leven met te veel ijzer
Prof. dr. J. J. M. Marx
Leven zonder ijzer is op aarde niet mogelijk. Bij de mens is de grootste hoeveelheid ijzer nodig voor de vorming van de rode bloedkleurstof, de hemoglobine, die zorgt voor het transport van zuurstof naar de weefsels. Bij een tekort aan ijzer wordt te weinig hemoglobine gevormd en ontstaat bloedarmoede ofwel anemie. Bijna elke leek weet dat je een dergelijke vorm van anemie goed kunt behandelen met staalpillen. IJzer is een essentieel bestanddeel van een zeer groot aantal eiwitten in het lichaam die een rol spelen bij de energievoorziening, de celdeling en de afweer tegen infecties.
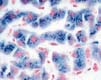 Het is veel minder bekend dat te veel ijzer in het lichaam ook klachten kan geven. De gevolgen van deze ijzerstapeling kunnen zelfs veel ernstiger zijn dan die van ijzergebrek. Cellen die te maken krijgen met een overmaat aan ijzer zijn aanvankelijk goed in staat om dit metaal op een veilige manier op te slaan in een hol eiwit, het ferritine, dat maximaal 5000 ijzeratomen in zijn binnenste kan herbergen. Op den duur kunnen de cellen al dat ijzer niet meer verwerken en gaat ijzer reageren met zogenaamde zuurstofradicalen waardoor het uiterst schadelijke hydroxylradicaal wordt gevormd. Dit stofje reageert vrijwel onmiddellijk met moleculen in de directe omgeving, waardoor zowel de celmembraan, eiwitten als de erfelijke substantie DNA beschadigd kunnen worden. Welke cellen schade oplopen hangt af van de oorzaak van de ijzerstapeling, en dat zijn er vele. Eigenlijk kan elke vorm van bloedarmoede die niet het gevolg is van een ijzertekort ijzerstapeling tot gevolg hebben.
Het is veel minder bekend dat te veel ijzer in het lichaam ook klachten kan geven. De gevolgen van deze ijzerstapeling kunnen zelfs veel ernstiger zijn dan die van ijzergebrek. Cellen die te maken krijgen met een overmaat aan ijzer zijn aanvankelijk goed in staat om dit metaal op een veilige manier op te slaan in een hol eiwit, het ferritine, dat maximaal 5000 ijzeratomen in zijn binnenste kan herbergen. Op den duur kunnen de cellen al dat ijzer niet meer verwerken en gaat ijzer reageren met zogenaamde zuurstofradicalen waardoor het uiterst schadelijke hydroxylradicaal wordt gevormd. Dit stofje reageert vrijwel onmiddellijk met moleculen in de directe omgeving, waardoor zowel de celmembraan, eiwitten als de erfelijke substantie DNA beschadigd kunnen worden. Welke cellen schade oplopen hangt af van de oorzaak van de ijzerstapeling, en dat zijn er vele. Eigenlijk kan elke vorm van bloedarmoede die niet het gevolg is van een ijzertekort ijzerstapeling tot gevolg hebben.
De ijzerstapelingsziekte die momenteel het meest in de belangstelling staat is de erfelijke aandoening hereditaire hemochromatose. De ziekte werd in de vorige eeuw ontdekt en beschreven als een vorm van suikerziekte die gepaard ging met een bruine verkleuring van de huid, “diabète bronzé”. Pas in de jaren vijftig werd bekend dat de ziekte behandeld kon worden door middel van aderlatingen.
Kenmerkend voor de ziekte is dat het transporteiwit transferrine in het bloed veel meer ijzer meedraagt dan bij normale personen. Het ferritine, een eiwit dat eigenlijk in de cel thuishoort, is in het bloed ook verhoogd. De ziekte ontstaat doordat het lichaam voortdurend meer ijzer opneemt uit de voeding dan nodig is. Het “oververzadigde” transferrine wordt nog voordat de grote circulatie bereikt wordt, via de poortader afgegeven aan de levercellen. De lever is dan ook het eerste orgaan dat bedreigd wordt bij hereditaire hemochromatose. Pas daarna wordt ijzer gestapeld in onder andere de alvleesklier, het hart en de huid.
De wijze van overerving is nog maar twintig jaar bekend en in 1996 werd een erfelijke afwijking (mutatie) gevonden van het pas ontdekte HFE-gen dat verantwoordelijk is voor het ontstaan van de ziekte. Hemochromatose is bij blanken de meest voorkomende “autosomaal recessieve” erfelijke aandoening: de aandoening is niet geslachtsgebonden en je moet de mutatie van beide ouders erven om zelf ziek te worden, dat wil zeggen je moet homozygoot zijn.
Mensen die de mutatie slechts van één ouder erven (heterozygoten) zijn gezond en hebben vrijwel nooit afwijkingen bij laboratoriumonderzoek. Opmerkelijk is echter dat de klachten en afwijkingen van hemochromatose bij homozygoten uiterst verschillend kunnen zijn. Sommigen krijgen al op jonge leeftijd ernstige littekenvorming van de lever en hebben zelfs een verhoogde kans om te overlijden aan leverkanker, zijn moe, krijgen suikerziekte, gewrichtsklachten en hartzwakte en zijn impotent. Anderen, met precies dezelfde erfelijke afwijking, hebben zelfs op hoge leeftijd geen enkele klacht of afwijking die kan samenhangen met hemochromatose. Sterker nog, ongeveer 10 procent van de patiënten met het typische beeld van hereditaire hemochromatose hebben helemaal geen mutatie van het HFE-gen en meestal komt dan in de familie ook geen hemochromatose voor. De typische gewrichtsklachten komen slechts voor bij ongeveer de helft van de patiënten en verbeteren nauwelijks tijdens behandeling met aderlatingen, terwijl de andere helft absoluut geen gewrichtsklachten heeft.
Er wordt, met name in het Academisch Ziekenhuis Utrecht, veel wetenschappelijk onderzoek verricht om al deze verschillen te verklaren. Ook wordt onderzocht of er bij heterozygoten afwijkingen kunnen ontstaan. Mocht dat inderdaad het geval zijn, en er zijn reeds aanwijzingen voor een grotere kans op bepaalde hart- en vaatafwijkingen, dan kan dit een argument zijn om op grote schaal bevolkingsonderzoek te doen. Niet minder dan een op de tien Nederlanders is immers drager van de erfelijke afwijking voor hemochromatose. Het gaat dan niet alleen om het opsporen van homozygoten, bij wie ziekteverschijnselen bij tijdige diagnose volledig voorkomen kunnen worden, maar ook om het vinden van heterozygoten. Een kosten-batenafweging zal hoogstwaarschijnlijk gunstig uitvallen voor een dergelijk zeer kostbare screening indien ook bij heterozygoten een positief effect op de levensverwachting aannemelijk wordt. De behandeling is niet moeilijk. Het is voldoende om donor te worden van de bloedtransfusiedienst. Het tekort aan donoren in Nederland is dan ook voor eens en altijd opgelost.